Les mécanismes d’action diffèrent de ceux des traitements classiques, tout comme les effets physiologiques donnés et les résultats cliniques.
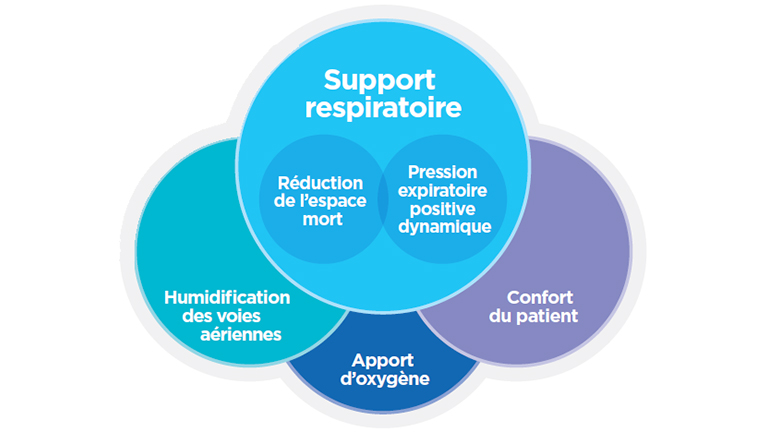
Les mécanismes d’action du traitement par haut débit nasal Optiflow sont :
- un support respiratoire (grâce à la réduction de l’espace mort et à la génération d’une pression positive dynamique des voies aériennes)
- une hydratation/humidification des voies aériennes
- le confort du patient
- l’apport d'oxygène (selon les besoins)
Remarque : les mécanismes d’action du haut débit ci-dessus s’appliquent à l’administration par une interface nasale Optiflow. Les mécanismes d’action sont différents si le haut débit est administré par trachéotomie ou par un adaptateur pour masque.
Explications sur la réduction de l’espace mort
La clairance de l’air expiré dans les voies aériennes supérieures réduit la réinhalation d’air à forte teneur en
CO2 et réduite en O2, ce qui entraîne une augmentation de la ventilation alvéolaire.
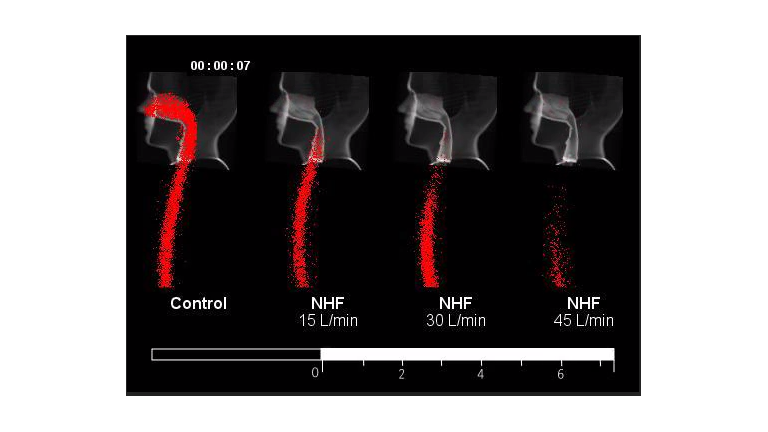
Réduction de l'espace mort
Voir les effets en action (45 secondes)
Cette vidéo montre la clairance d'un traceur radioactif dans un modèle des voies aériennes supérieures à l’aide d’une l’imagerie à caméra gamma avec une tomodensitométrie. Les débits étaient de 15, 30 et 45 L/min. Dans cette expérience, vous pouvez constater que la clairance augmente à mesure que le débit augmente.
Explications sur la pression positive dynamique des voies aériennes
Le haut débit nasal crée une pression dépendante de la respiration et du débit, facilitant
l’inspiration et favorisant une respiration lente et profonde à l’expiration, augmentant ainsi
la ventilation alvéolaire.
Pression positive dynamique des voies aériennes
Voir les effets en action (33 secondes)
Corley et al. 2011 ont montré que dès l’administration du traitement Optiflow chez les patients ayant subi une intervention chirurgicale cardiaque, on constate une augmentation significative de l’aération des poumons. Ce changement reflète une augmentation du volume pulmonaire et du volume courant. Les chercheurs ont identifié une forte corrélation entre la pression dans les voies aérienne (Paw) et l’impédance
pulmonaire de fin d’expiration (EELI). La Paw a augmenté de 3,0 cmH2O et l’EELI a augmenté de 25,6 %. L’EELI est une mesure de substitution du volume pulmonaire de fin d’expiration.
Explications sur l’humidification des voies aériennes
L’humidité permet une administration confortable des hauts débits. Une humidité optimisée favorise l’équilibre naturel entre la chaleur et l’humidité présentes en temps normal dans des poumons sains et peut participer au maintien de la stabilité physiologique des voies aériennes compromises.
Humidification des voies aériennes
Voir les effets en action (45 secondes)
L’expérience présentée dans la vidéo a été réalisée sur deux échantillons de trachée d’ovins, l’un exposé à 100 % d’humidité relative (partie gauche) et l’autre à 90 % d’humidité relative (partie droite) pendant 15 minutes.
Au démarrage de la vidéo, les petits cils battent à l’arrière-plan. Ensuite, les débris dans le mucus de l’image de droite deviennent stationnaires. Les points sombres se déplaçant rapidement dans l’image de gauche ont montré que les débris sont évacués par un transport mucociliaire efficace. Après seulement une heure à la plus faible humidité, la muqueuse s’est complètement desséchée.
Explication sur le confort du patient
L’assistance respiratoire administrée par un masque présente des difficultés pour les cliniciens et les patients. Le Haut Débit Nasal (NHF) est administré par une interface nasale. Un meilleur confort du patient peut favoriser une plus grande observance.

Confort du patient
Les données cliniques suggèrent que l’utilisation du traitement Optiflow augmente le confort comparé aux dispositifs d’apport d’oxygène classiques1,2. Une étude dans le JAMA3 a montré que le traitement Optiflow a entraîné une réduction significative des lésions cutanées et a réduit la charge de travail du personnel infirmier par rapport à la BIPAP. Les patients peuvent manger, boire et dormir avec l’interface Optiflow et peuvent parler avec leurs soignants et leur famille.
1. Roca et al. Respir Care. 2010.
2. Lenglet et al. Respir Care. 2012.
3. Stéphan et al. JAMA. 2015.
Explication sur l’apport d'oxygène (selon les besoins)
Fournir de l’oxygène par Haut Débit Nasal (NHF) peut faciliter la précision de l’administration
d’un mélange air/oxygène humidifié.
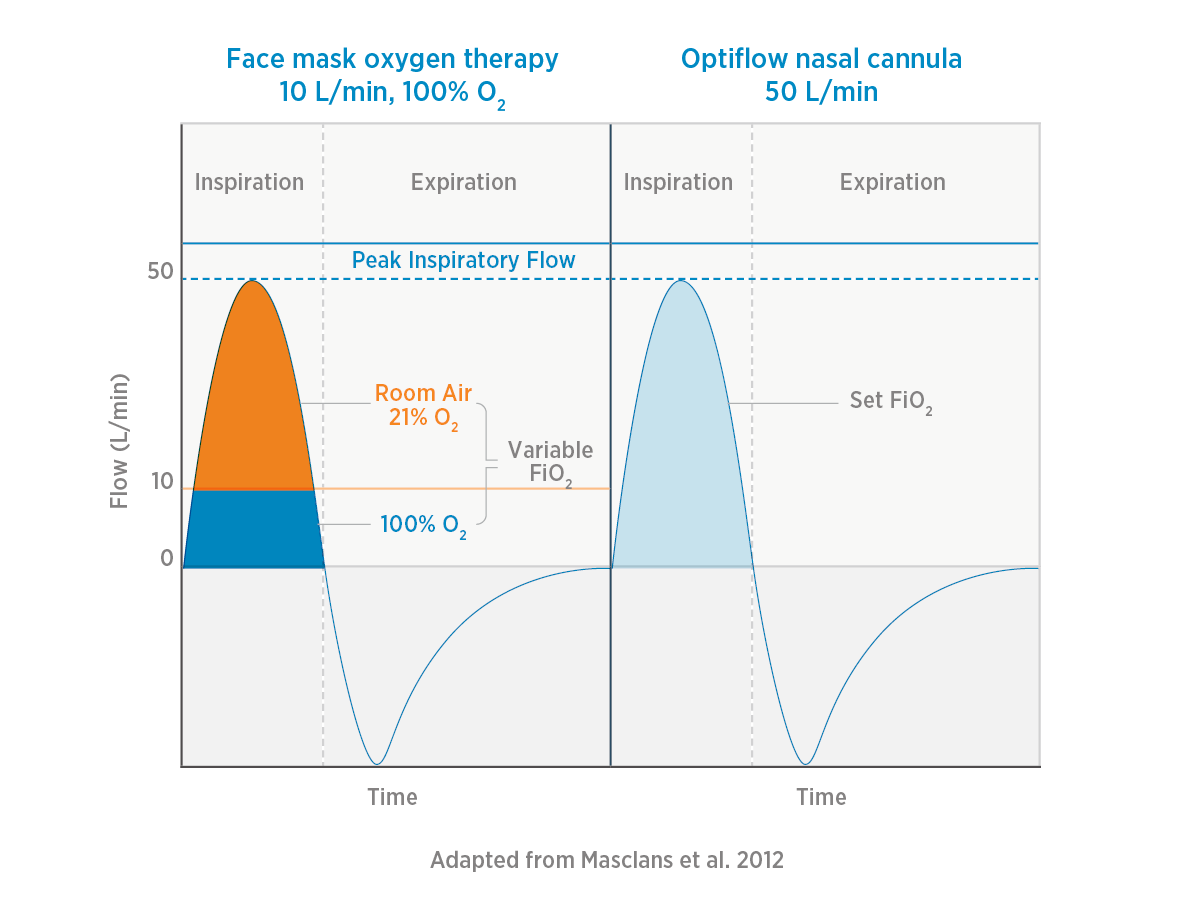
Apport d’oxygène
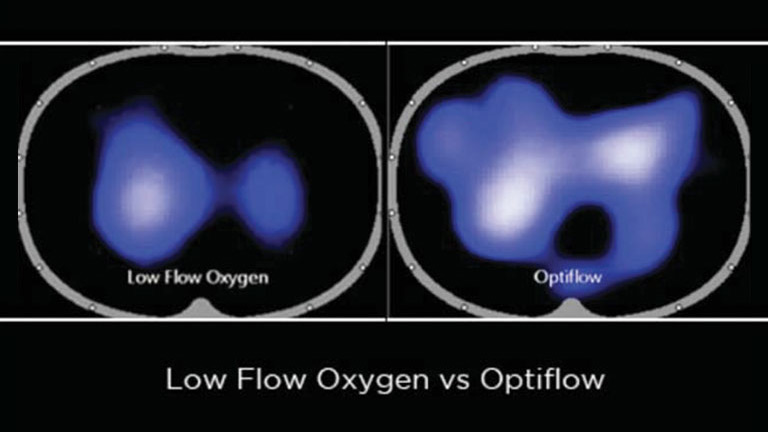
Dans l’exemple illustré dans la partie gauche de l’écran, le débit d’oxygène maximal du masque à oxygène (partie gauche) est limité à environ 10 L/min, ce qui ne suffit pas pour couvrir la demande inspiratoire de pointe du patient de 50 L/min. Pour compenser ce déficit, 40 L/min d’air ambiant sont pris à chaque inspiration, ce qui dilue l’oxygène et administre une FiO2 variable (et parfois inconnue).
Dans notre exemple (partie droite), l'Optiflow est capable de couvrir la demande inspiratoire totale du patient de 50 L/min, sans dilution de l’oxygène, ce qui facilite l’administration d’une FiO2 spécifique.
DPM-189